История открытия водорода
Доподлино установить кто открыл водорода невозможно, поскольку он известен с XVI века. Алхимики заметили, что при взаимодействии железных опилок с соляной или серной кислотой выделяется «горючий воздух», или «искусственный воздух». Однако его все-таки считали воздухом, получившим почему-то способность гореть.
Но вот сторонник точных измерений Генри Кавендиш (Henry Cavendish) выделил водород из серной и соляной кислот железом, цинком, оловом. Он собирал его в газометре и узнал, что при горении «горючего воздуха» образуется чистая вода. Поэтому считается, что лавры открытия водорода принадлежат именно ему.
Однако окончательное суждение о «горючем газе», так же как и о кислороде, принадлежит Антуану Лорану Лавуазье (Antoine Laurent de Lavoisier). Он повторил опыт Кавендиша, поставил новые опыты и доказал, что «горючий воздух» — это простое вещество, что вода не простое тело, а химическое соединение двух элементов — водорода и кислорода. Лавуазье дал имя «горючему воздуху» hydrogene (от греч. «рождающий воду») .
Интересны первые русские наименования водорода: «водотворный газ», «водотвор». Легкость водорода, пожалуй, поразила первых наблюдателей больше, чем остальные его свойства. Думали даже, что он и есть тот таинственный с «отрицательным весом» флогистон, который, проникая в тела, сообщает им способность гореть.
В 1794 г. к водороду возник чисто военный интерес. В то время уже были изобретены воздушные шары, наполненные горячим воздухом, — монгольфьеры Их называли так в честь братьев французов Монгольфье, совершивших первый полет на таком аэростате в 1783 г.
Преимущества водорода перед нагретым воздухом были очевидны. Нагретый воздух обладал подъемной силой, пока он не остывал до температуры окружающего воздуха. Следовательно, чтобы совершить более или менее длительный полет, надо было под отверстием аэростата в гондоле пилота поддерживать огонь, подогревать воздух. Конечно, это было опасно и приводило к трагическим катастрофам. А водород всегда будет легче воздуха более чем в 14 раз. И его не надо нагревать, наоборот — беречь от огня.
Лавуазье разработал промышленный способ получения водорода, названный «железо-паровым». Заключался он в следующем. Пары воды из котла поступали в железные трубы, наполненные железными стружками. Трубы накалялись в жаровнях — протекала химическая реакция вытеснения водорода железом из воды с образованием железной окалины:
3Fe + 4Н2O = Fe3O4 + 4Н2
Избыток водяных паров, непрерывно поступающих в трубу, проходил через холодильник, а водород по трубам направлялся в аэростат и надувал его.
Когда железо израсходуется, его опять можно получить из накаленной окалины, если через трубу пропустить светильный газ. Уравнение показывает, что 3?56=168 г железа могут вытеснить 8 г водорода, или 4?22,4=89,6 л водорода.
В войнах 1904-1905 и 1914-1918 гг. привязанные канатами аэростаты служили главным образом для наблюдения за прицельностью артиллерийского огня, за передвижением войск. Во время Великой Отечественной войны 1941-1945 гг. они защищали военные объекты от авиации противника. Летчики, опасаясь столкновений с аэростатом и канатами, летали на большой высоте, поэтому их бомбовые удары в значительной мере теряли прицельность.
Первый в мире полет на аэростате с научной целью совершил ученый Захаров Яков Дмитриевич в 1804 г. А в 1887 г. для наблюдения солнечного затмения и изучения воздуха поднялся в воздух Менделеев Дмитрий Иванович.
Эксплуатация
После сборки можно начинать испытания прибора. Для этого на конце трубки устанавливают горелку из медицинской иглы и начинают заливать воду. В воду нужно добавить KOH или NaOH. Вода должна быть дистиллированная или талая на крайний случай. Для работы устройства достаточно 10% концентрации щелочного раствора.
Читать далее: Как сделать умывальник для дачи своими руками пошаговый инструктаж
После этого к электродам по схеме подсоединяют ЛАТР с диодным мостом. В цепь устанавливают амперметр и вольтметр для контроля работы. Начинают с минимального напряжения и потом постоянно увеличивают, наблюдая за газовыделением.
Предварительно работы лучше проводить на открытом воздухе вне дома
Поскольку установка взрывоопасна, все работы следует проводить с особой осторожностью
При испытаниях наблюдают за работой прибора. Если имеет место маленькое пламя горелки, то может быть или низкое газовыделение в генераторе, или где-то происходит утечка газа. Если раствор помутнел, грязный, его нужно заменить. Также необходимо следить, чтобы прибор не перегревался, а вода не закипела.
Польза ионизированной воды
О пользе ионизаторов щелочной воды известно многим потребителям, но только недавние клинические исследования определили, какие именно свойства воды имеют терапевтический эффект.
Только после 2007 года ученые обнаружили, что терапевтическое свойство в щелочной ионизированной воде представляет собой газообразный водород Н2. Поэтому для терапевтического эффекта важна концентрация Н2 в воде.
Изначально производители ионизирующих приборов акцентировали свое внимание на показатели щелочной среды, а не на газообразный водород. Поэтому есть 3 наблюдения щелочных систем:
- Некоторые ионизаторы воды не содержат достаточного количества растворенного газообразного водорода или, по меньшей мере, их концентрация ниже предела обнаружения 0,01 мг/л.
- Некоторые ионизаторы воды способны создавать достаточные уровни Н2, но их электродах образуется налет, что значительно сокращает концентрацию газа Н2 в воде. Поэтому, не очищая системы лимонной кислотой или уксусом, концентрация Н2 также может опускаться ниже 0,01 мг/л в течение нескольких дней в зависимости от качества использованной воды.
- Некоторые ионизаторы воды используют технологию обратной полярности, которая значительно предотвращает образование накипи на электродах, что позволяет пользователю работать дольше (от нескольких месяцев до нескольких лет) без использования уксуса или лимонной кислоты.
При всех обстоятельствах концентрация Н2 сильно зависит от исходной воды и расхода (и, конечно, от конструкции и количества скейлинга на электродах). Это приводит к тому, что концентрация варьируется от менее 0,01 мг/л до почти 3 мг/л, при этом среднее значение составляет от 0,4 до 1 мг/л при условии среднего качества исходной воды и чистых электродах.
Важно также отметить, что, хотя некоторые ионизаторы воды могут создавать очень высокую концентрацию Н2 за счет замедления потока воды, эта продуцируемая вода часто имеет очень высокий уровень рН, что может сделать воду неприемлемой. В этом случае легко снизить pH путем добавления нескольких капель лимонного сока (лимонной кислоты) для снижения рН при сохранении более высокого уровня, растворенного Н2
4 способа получения водорода
Существует более 100 различных методов добычи гидрогена – как теоретических, так и освоенных в промышленных масштабах. В зависимости от выбранного вами вида получения ресурса, производство водорода потребует различного оборудования, сырья и других ресурсов.
Рассмотрим 5 самых распространенных способов производства водорода.
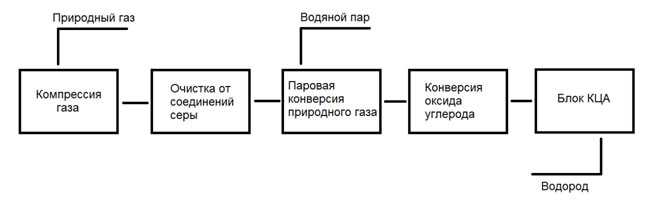
Способ №1. Паровая конверсия
Более 50% всего водорода получается путём паровой конверсии воды и метана. При этом три основных составляющих (природный газ, водяной пар и оксиген) смешиваются в определённых пропорциях.
Таким образом, часть природного газа сгорает вместе с кислородом, тем самым поддерживая необходимую температуру для продолжения химической реакции. Метан, не выгоревший во время реакции конверсии, реагирует с водяным паром, образуя оксид углерода (то есть сажу) и непосредственно гидроген.
Простота и относительная лёгкость делает производство водорода путём паровой конверсии наиболее дешёвым из всех доступных.
Способ №2. Разделение метана на углерод и водород
Благодаря дешевизне метана, а также простому способу его получения, такой тип добычи водорода проще всего. Однако высокие температуры и потенциальная пожароопасность требуют дополнительных мер безопасности. К тому же, оборудование для полного процесса крекинга не из дешёвых.
Способ №3. Электролиз воды
Ещё один вид добычи гидрогена – электролиз воды. Это второй по распространённости метод добычи водорода, обеспечивающий достаточно высокую чистоту конечного продукта. Сопутствующим «бонусом» в этом технологическом процессе становится кислород, не менее важный элемент.

Для такого способа производства требуются значительные запасы воды. Тем не менее он совсем не требователен к её качеству – для электролиза можно использовать промышленную, дождевую или даже сточную воду.
Способ №4. Пиролиз
«Топливом» для этого могут служить отходы сельского хозяйства и пищевых производств:
- Птичий помёт и другие побочные продукты животноводства.
- Отходы рыбных, соко- и мясокомбинатов.
- Некоторые виды технических культур, специально выращенных для получения биомассы.
При переработке всех этих биоотходов при помощи специальных бактерий образуется синтез-газ, в основном состоящий из двуокиси карбона и метана. Продуктом их переработки и становится гидроген.
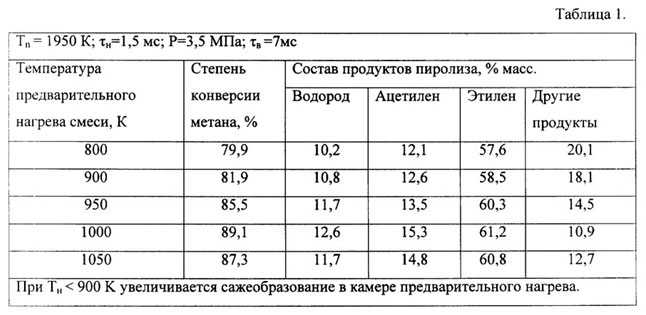
Такой способ производства набирает всё большую популярность ввиду того, что, помимо гидрогена, из биомассы добываются этилен и ацетилен. Также ценным сырьём являются и сами биоотходы, которые широко используются в сельском хозяйстве для производства удобрений.
Особенности использования водорода
Одноатомный водород является самым распространенным химическим элементом не только на Земле, но и во Вселенной. Он легко взаимодействует с большинством неметаллов, поэтому основная его часть связана в воде и органических соединениях.
В промышленности водород получают несколькими способами: большую часть – при переработке угля, газа и нефти, и только 4% – при электролизе воды (так называемый зеленый водород).
Получается, что топливо – вода, источник водорода для водородного генератора, достается вообще бесплатно или за символическую сумму. А если собрать прибор самостоятельно, то можно получить потрясающую экономию.
Но на практике все не так радужно. Молекула воды состоит из двух атомов водорода и атома кислорода. Связь между атомами прочная, и, чтобы разорвать ее, нужен внешний источник энергии. Самым удобным источником является электроэнергия, самый выгодный процесс – электролиз.

Сферы использования водородаИсточник ppt-online.org
В промышленных установках реализуется замкнутый цикл, когда водяной пар возвращается в жидкое состояние (конденсируется). Для получения конденсата водяной пар охлаждают, а это означает дополнительные затраты энергии. Газ, произведенный промышленным способом, используется в разных целях, поэтому имеет разную степень очистки. Водород с низкой степенью очистки применяется в сварочном оборудовании, хорошо очищенный – в качестве топлива.
Получение водорода
В промышленности технический водород получают:
- электролизом воды;
- методом глубокого охлаждения газовых смесей, содержащих водород;
- железо-паровым способом;
- из водяного газа путем окисления содержащейся в нем окиси углерода водяным паром в присутствии катализатора;
- в специальных водородных генераторах воздействием серной кислоты на железную стружку и цинк.
Получение водорода из кислот
На первых порах источником для получения водорода служили кислоты. Так и в наше время в лабораториях часто получают его средневековым способом — действием цинка на серную кислоту. Реакция протекает по уравнению:
Zn + H2SO4 = ZnSO4 + H2
Вместо цинка можно взять железо в виде стружек или алюминий. Водород получается, загрязненный побочными продуктами разложения серной кислоты, и, если это требуется, его приходится очищать.
Добыча водорода из промышленных газов
Огромные количества водорода, необходимые современной промышленности, получают сейчас электролизом раствора щелочи и извлекают из промышленных газов — коксовальных печей, газов, получаемых при переработке нефти и др.
При переработке каменного угля на кокс дополнительно получается деготь и коксовый газ. В состав газа входит до 50-60% водорода (H2), 20-25% метана (СН4), окись углерода (СО), азот (N) и др.
В статье о свойствах гелия и способах его производства описан процесс получения гелия методом фракционной конденсации. Так же поступают и с коксовым газом. Но чтобы отделить водород от других составных частей, требуется очень глубокое охлаждение из-за низкой критической температуры водорода.
Производство водорода из воды
Наиболее широко распространенным способом производства водорода является — электролиз дистиллированной воды. В результате чего получают водород, кислород и некоторые примеси.
Единственным исходным сырьем для добычи водорода электролитическим методом служит вода. Чистая, дистиллированная вода обладает огромным сопротивлением и почти совершенно не проводит электрический ток. Вот почему для того чтобы сделать воду электропроводной, в ней нужно растворить какую-нибудь соль, кислоту или основание, которые дают ионы.
Через водный раствор щелочи (например: каустическая сода) пропускают постоянный электрический ток. При этом вода разлагается, и на отрицательном электроде (катоде) выделяется водород, а на положительном электроде (аноде) — кислород, также являющийся важным промышленным продуктом.
Большой расход электроэнергии является главным недостатком данного способа, поэтому применение водорода полученного при помощи электролиза целесообразно при одновременном использовании вместе с кислородом. В связи с этим в последнее время портативные водородные сварочные аппараты для газовой сварки и пайки пользуются все большей популярностью.
Характеристика водорода
Характеристики H2 представлены в таблицах ниже:
Водород в баллоне
| Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м3) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
| H2 | 40 | 0,54 | 6,0 |
Благодаря этой таблице теперь можно легко дать ответы на вопросы, которые очень часто задают сварщики:
- Сколько кубов (м3) водорода в 40 литровом баллоне? Ответ: 6,0 м3
- Сколько кг водорода в баллоне?Ответ: 0,54 кг
- Сколько весит баллон с водородом?Ответ:
58,5 кг — масса пустого баллона из углеродистой стали согласно ГОСТ 949;
0,54 — кг масса водорода в баллоне;Итого: 58,5 + 0,54 = 58,94 кг вес баллона с водородом.
Рекомендуем к просмотру видео об открытии водорода, его характеристиках и производстве.
Применение водорода
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 оС. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.

В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
- В лаборатории водород получают действием кислот на металлы.
- В промышленности для получения водорода используют доступное и дешевое сырье — природный газ, воду.
- Водород — это перспективный источник энергии XXI в.
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Создан наиболее эффективный метод получения водорода
Lisa Smith/Institute for Solid State Physics and Optics
Международная группа ученых создала катализатор, который позволяет получить водород из воды, затрачивая вдвое меньше энергии, чем раньше. Статья об этом появилась на страницах журнала Nature Communications.
Электролиз традиционно применяется для получения водорода из воды. При этом процессе через воду пропускается электрический ток, в результате чего происходит реакция ее разделения на водород и кислород. Если электрический ток для процесса электролиза генерируется с помощью возобновляемых источников энергии, таких как ветер или солнечная энергия, то при нем не происходит никаких выбросов углекислого газа.
Затем водород может использоваться в качестве источника топлива с нулевым выбросом в некоторых видах транспорта, таких как автобусы и автомобили, или для отопления жилых домов. Но пока что получение водорода оказывается экономически не слишком выгодным, так как потери электроэнергии при электролизе довольно велики.
Чтобы уменьшить затраты на получение водорода, ученые из Университета Глазго, Кильского и Лиссабонского университетов создали новый катализатор для этой реакции. Катализаторы ускоряют химические реакции, понижая необходимую для их начала энергию. Новый материал представляет собой слои теллурида молибдена MoTe2, которые покрывают электроды.
По словам ученых, в обычных условиях этот материал проявляет небольшую каталитическую активность, но его характеристики значительно улучшаются при использовании катодного смещения. Так, ученым удалось обнаружить, что при сохранении постоянной плотности тока — величины, которая определяет выход водорода в электрохимической реакции, — возможно уменьшить подаваемое напряжение в два раза, с 320 милливольт до 178.
Источник
Будущее применение
Топливные элементы считаются ключом как будет использоваться энергия водорода в будущем, поскольку они могут преобразовывать его непосредственно в электрическую энергию. Теоретически это приводит к более высокой эффективности, чем при сжигании в обычных тепловых электростанциях.
Принцип работы топливных элементов известен уже очень давно.
Есть некоторые споры о том, кто на самом деле изобрел топливный элемент:
- Немецко-швейцарский химик Кристиан Фридрих провел первые тесты в технологии топливных элементов в 1838 году.
- Английский физик сэр Уильям Роберт Гроув построил первый топливный элемент в 1839 году.
- Впоследствии такие известные ученые, как Анри Беккерель и Томас Эдисон, стали участвовать в их дальнейшем развитии. Однако это была довольно слабо продвинутая стадия развития.
- Наконец, в середине двадцатого века была достигнута задача, позволившая применение и основное использование топливных элементов.
Топливные элементы, в основном, предполагают реверсирование электролиза. Топливный элемент всегда содержит два электрода. В зависимости от типа топливного элемента, чистый водород (H2) или топливо содержащее углеводороды подают через анод и чистый кислород (О2 ) или воздух в качестве окислительного материала через катод. Электролит отделяет анод и катод. Электроны текут по большой цепи и создают электрическую энергию.
С 1990-х годов разработка топливных элементов идет полным ходом. Автомобильные производители и энергокомпании приняли технологию и ищут способ получить прибыль от положительного применения водорода как источника энергии.
Биологическое производство водорода
Одним из наиболее известных организмов, используемых в биологическом производстве водорода, является бактерия Enterobacter aerogenes. Этот микроорганизм может использовать различные органические вещества (например, глюкозу, целлюлозу, лактозу) в качестве источника энергии и питательных веществ для своего роста и размножения.
Процесс биологического производства водорода основан на анаэробных (без кислорода) условиях, так как кислород может уничтожить микроорганизмы. Бактерии, используя ферменты, разлагают органические вещества, выделяя водород и углекислый газ. Водород может быть использован в различных сферах промышленности, включая производство энергии, производство аммиака и водородных топливных элементов.
Подобные процессы биологического производства водорода могут быть улучшены путем генной инженерии организмов. Исследователи ищут способы усилить активность ферментов, ответственных за разложение органических веществ и выделение водорода. Такие улучшенные организмы могут позволить повысить эффективность процесса и уменьшить затраты на его осуществление.
Биологическое производство водорода имеет ряд преимуществ по сравнению с традиционными методами получения водорода, основанными на использовании ископаемого топлива. Во-первых, данный процесс не является энергозатратным, так как микроорганизмы осуществляют биологическую реакцию сами по себе. Во-вторых, процесс происходит при низких температурах и низком давлении, что позволяет избежать проблем связанных с высокой температурой и давлением, которые требуются при традиционных методах. Наконец, процесс биологического производства водорода является экологически чистым, так как в качестве побочных продуктов выделяются только вода и углекислый газ, которые не наносят вред окружающей среде.
Применение водорода
Основными направлениями применения водорода являются:
- химическая промышленность – синтез аммиака, метанола, углеводородов;
- пищевая промышленность – получение пищевых белков;
- нефтехимия – нефтепереработка (гидрогенезационная очистка нефтепродуктов);
- автотранспорт – автомобили на газообразном и жидком водороде;
- машиностроение – для сварки и резки металлов.
Применение водорода в сварке
Водород использовался в качестве защитного газа еще при первых попытках защиты дугового пространства от воздуха. Однако водород может оказать в ряде случаев вредное воздействие. Это объясняется тем, что при применении водорода в металле сварных швов образуются дефекты в виде пор, а также является одним из главных факторов образования холодных трещин. С увеличением толщины свариваемых элементов пористость в металле сварных швов становится значительной. Поэтому его использование в дальнейшем было значительно ограничено. В чистом виде (и в виде водородно-азотных смесей, получаемых при диссоциации аммиака) он в настоящее время применяется при атомно-водородной сварке (хотя и сам этот способ заменен теперь другими, в частности сваркой неплавящимся электродом).
Если струю водорода пропускать через пламя вольтовой дуги, то водород диссоциирует на атомы с поглощением значительного количество тепла (103,6 ккал/моль) что приводит к значительному увеличению напряжения дуги. Она становится устойчивой только при повышении напряжения источника тока. Так, например, при режимах атомно-водородной сварки наиболее эффективной «звенящей» дугой при вольфрамовых электродах и силе тока 10-20 А напряжение дуги составляет около 100 А, напряжение холостого хода питающего источника должно быть не менее 200-220 В (обычно около 300 В). В этом случае водород является не только защитным газом, но и переносит тепловую энергию из дуги на поверхность не включенного в цепь тока изделия.
Образовавшийся атомный водород направляют на твердую свариваемую поверхность, где происходит нагревание и расплавление металла за счет поглощения тепла, которое выделяется при рекомбинации атомов до молекулярного водорода. Ассоциация атомарного водорода на холодной поверхности металла (в том числе и расплавленной, так как температура плавления большинства металлов ниже температуры возможного существования заметных количеств атомарного водорода) приводит к выделению тепла, потребленного в дуге на диссоциацию. За счет выделяющегося тепла температура свариваемой поверхности металла повышается до 3528-4028°С. Такая атомно-водородная сварка позволяет обрабатывать и сваривать самые тугоплавкие металлы, высококачественные стали, коррозионно-устойчивые материалы, цветные металлы.
Несмотря на то, что атмосфера, окружающая металл, при атомно-водородной сварке представляет собой смесь молекулярного и атомарного водорода, при отсутствии на металле значительного количества окислов швы получаются достаточно плотными и применительно к низкоуглеродистой стали не имеют большого количества диффузионно-подвижного и остаточного водорода.
При струйной защите иногда используется водяной пар. Однако в этом случае получается значительно меньшая стабильность качества сварных швов, чем при сварке с защитой дуги углекислым газом. В связи с этим такой процесс широкого распространения не получил.
При TIG сварке аустенитной нержавеющей стали с целью увеличения напряжения дуги, увеличения теплоэффективности и снижения оксидирования используют аргоно-водородные смеси газов (15% Н2). Более высокая температуру и сжатие дуги, в свою очередь увеличивает глубину проплавления металла. Однако при этом необходимо учитывать возможность вредного влияния растворяющегося в металле водорода. Более широко водород применяют в специальных областях сварки и металлургии, например в порошковой металлургии при спекании изделий из порошковых материалов.
В других случаях применение водорода и водородосодержащих газов, как защитных при дуговой сварке, нецелесообразно.
Применяют водород для составления плазмообразующих смесей при плазменной сварке и резке. Так, для защиты сварочной ванны от окисления при плазменной сварке легированной стали, меди, никеля и сплавов на его основе используют смесь аргона с 5-8% водорода.
Аргоно-водородную смесь, имеющую до 20% Н2, применяют при микроплазменной сварке. Наличие водорода в смеси обеспечивает сжатие столба плазмы, делает его более сконцентрированным. Кроме того, водород создает необходимую в ряде случаев восстановительную атмосферу.
Приборы электролиза воды
На рынке существует множество приборов и устройств, способных изменять химические и физические показатели воды. Современная наука научилась определять какие именно показатели воды имеют полезные и терапевтические свойства. Данная статья расскажет о приборах, которые делают влияют на показатели воды и какие показатели имеют ключевые функции.
В настоящее время большая популярность двух методов получения ионизированной воды, это электрические системы, которые влияют на воду через высокое содержание солей в воде, а именно, ионизаторы щелочной воды и генераторы водородной воды с нейтральным рН. Для начала давайте рассмотрим ионизаторы щелочной воды.
Примечания[ | ]
- Немецкая волна 17.09.2018 Инза Вреде Поезд на водороде — европейский технологический прорыв с оговорками
- «Перепись ВОДОРОДА» Журнал «Газпром», сентябрь 2020, стр 42
- ↑ 12Da Rosa, Aldo Vieira. Fundamentals of renewable energy processes. — Amsterdam: Elsevier Academic Press, 2005. — С. 370. — xvii, 689 pages с. — ISBN 0120885107.
- Novel sugar-to-hydrogen technology promises transportation fuel independence | Virginia Tech News | Virginia Tech
- nanoHUB.org — Topics: Aluminum-Rich Bulk Alloys: an Energy Storage Material for Splitting Water to Make Hydrogen Gas on Demand
- Hydrogen production using hydrogenase-containing oxygenic photosynthetic organisms (англ.). Дата обращения 17 октября 2019.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
Добыча водорода в условиях домашнего хозяйства
Выбор электролизера
Для получения элемента дома необходим специальный аппарат – электролизер. Вариантов такого оборудования на рынке много, аппараты предлагают как известные технологические корпорации, так и мелкие производители. Брендовые агрегаты дороже, но качество их сборки выше.
Домашний прибор отличается малыми габаритами и легкостью в эксплуатации. Основными деталями его являются:
Электролизер — что это
- риформер;
- система очистки;
- топливные элементы;
- компрессорное оборудование;
- емкость для хранения водорода.
В качестве сырья берется простая вода из-под крана, а электричество идет из обычной розетки. Сэкономить на электроэнергии позволяют агрегаты на солнечных батареях.
«Домашний» водород применяют в системах отопления или приготовления пищи. А также им обогащают бензовоздушную смесь, чтобы повысить мощность двигателей автомобиля.
Изготовление аппарата своими руками
Еще дешевле сделать прибор самому в домашних условиях. Сухой электролизер выглядит как герметичный контейнер, который представляет собой две электродные пластины в емкости с электролитическим раствором. Во Всемирной сети предлагаются разнообразные схемы сборки аппаратов разных моделей:
- с двумя фильтрами;
- с верхним либо нижним расположением контейнера;
- с двумя или тремя клапанами;
- с оцинкованной платой;
- на электродах.
Схема устройства электролиза
Простой прибор для получения водорода создать несложно. Для него потребуются:
- листовая нержавеющая сталь;
- прозрачная трубка;
- штуцеры;
- пластиковая емкость (1,5 л);
- водяной фильтр и обратный клапан.
Устройство простого прибора для получения водорода
Помимо этого, нужны будут различные метизы: гайки, шайбы, болты. Первым делом нужно распилить лист на 16 квадратных отсеков, у каждого из них спилить угол. В противоположном от него углу требуется высверлить отверстие для болтового крепления пластин. Для обеспечения постоянного тока пластины нужно подключать по схеме: плюс–минус–плюс–минус. Изолируют эти детали друг от друга с помощью трубки, а на соединении болтом и шайбами (по три штуки между пластинками). На плюс и минус насаживают по 8 пластин.
При правильной сборке ребра пластинок не будут задевать электроды. Собранные детали опускают в емкость из пластика. В месте касания стенок болтами делают два установочных отверстия. Устанавливают защитный клапан для удаления избытка газа. В крышку контейнера монтируют штуцеры и герметизируют швы силиконом.
Тестирование аппарата
Чтобы протестировать аппарат, выполняют несколько действий:
Схема получения водорода
- Наполняют жидкостью.
- Прикрыв крышкой, соединяют один конец трубки со штуцером.
- Второй опускают в воду.
- Подключают к источнику питания.
После включения прибора в розетку через несколько секунд будет заметен процесс электролиза и выпадение осадка.
Чистая вода не обладает хорошей электропроводностью. Для улучшения этого показателя нужно создать электролитический раствор, добавив щелочь – гидроксид натрия. Он есть в составах для очищения труб наподобие «Крота».
Производство
Водородная энергетика использует несколько способов производства водорода.
Газ сначала должен быть получен в чистом виде, прежде чем энергия из него может быть получена. Это требует легкодоступного недорогого сырья, содержащего этот химический элемент. Кроме воды (H2O), которая состоит из водорода (H) и кислорода (O) могут быть применены смеси углерода. Это в первую очередь природный газ или метан (CH4). Мазут и уголь также состоят из водорода (H) и углерода (C), но имеют гораздо более высокую долю углерода, чем природный газ.
Из углеводородов
Современные промышленные методы получения водорода почти исключительно используют ископаемые топливо, как природный газ, сырую нефть или уголь, как сырье. Такие методы, как паровой риформинг или частичное окисление паром для получения водорода из ископаемых углеводородов. Этот процесс химически отделяет углерод который после этого превращается в окись углерода (CO). Эти методы добычи водорода не являются идеальным вариантом с целью активной защиты климата. 
В основном, упомянутый способ производства водорода из ископаемых источников работает при высоких температурах обработки. Это требует большого количества внешних ресурсов.
Поэтому для получения водорода необходимы другие методы, с тем чтобы он был экологически чистым и безопасным. Идеальным способом является электролиз.
Методом электролиза
Немецкий химик Иоганн Вильгельм Риттер впервые использовал электролиз для получения водорода еще в 1800 году. С помощью электрической энергии, электролиз разлагает воду на водород и кислород. 
Особенностью электролиза может быть то, что если электроэнергия добыта из возобновляемых источников, то производство водорода во всем цикле может выделять только углекислый газ.
С помощью этого метода два электрода погружают в проводящий водный электролит. Это может быть смесь воды и серная кислота или гидроксид калия (KOH). Аноды и катоды проводят постоянный ток в электролитах и на них образуются газы водород и кислород. Хотя электролиз уже достиг высокого уровня технического развития, как экологически совместимый вариант производства кислорода, другие альтернативные методы также разрабатываются.
Термохимический метод
При температуре выше 1700° C вода непосредственно разлагается на водород и кислород.  Однако эти температуры требуют дорогостоящих термостойких средств. Необходимую температуру можно уменьшить ниже чем 1000° С через различные сопряженные химические реакции.
Однако эти температуры требуют дорогостоящих термостойких средств. Необходимую температуру можно уменьшить ниже чем 1000° С через различные сопряженные химические реакции.
Биологическое получение
Другие методы включают фотобиологическое производство водорода. Суть этого метода в том, что некоторые водоросли во время роста при нехватке серы производят водород.  Это типа биореакторов использующих свет для разложения воды.
Это типа биореакторов использующих свет для разложения воды.



























