Содержание
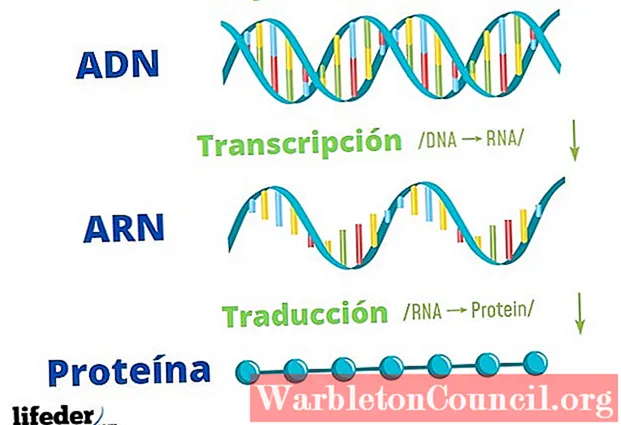
В центральная догма молекулярной биологии устанавливает общепринятые современные биологи критерии потока генетической информации в живых существах, включая как молекулы, так и процессы.
В конце концов, Догма делает акцент на необратимости потока биологической информации. Как только он проявится в виде пептидов, его нельзя вернуть. То есть поток генетической информации необратим и следует в направлении ДНК → Белки, но никогда не Белки → ДНК.
Однако история показала, что поток генетической информации в живых существах и вирусах намного сложнее этого.
Первоначальная «догма» была предложена Фрэнсисом Криком в 1950-х годах с точки зрения понимания процесса синтеза белка.
Мир
|
Фото: пресс-служба Нобелевского комитета |
|---|
6 октября оргкомитет назвал лауреата премии мира. Им за «борьбу против угнетения женщин и продвижение прав человека и свободы для всех» стала Наргес Мохаммади.
51-летняя иранская правозащитница начала свою деятельность еще в 1990-х. В разные годы она вела борьбу за отмену смертной казни, выступала против пыток и сексуального насилия в отношении политзаключенных, оказывала помощь активистам и их семьям. В Иране Мохаммади арестовывали 13 раз.
Сейчас правозащитница находится в тюрьме: в мае тегеранский суд приговорил ее к двум с половиной годам заключения, 80 ударам плетью и двум штрафам за «распространение пропаганды против государства». За все время своей деятельности активистка получила 31 год заключения и 154 удара плетью.
«Премия мира этого года также присуждается сотням тысяч людей, которые в предыдущем году выступили против режима, направленного на дискриминацию и угнетение женщин», — написано в пресс-релизе Нобелевского комитета.
9 октября станет известно имя лауреата в последней категории — по экономике.
ранняя жизнь и образование
Темин родился в Филадельфии, штат Пенсильвания, в семье евреев, активистки Аннет (Леман) и адвоката Генри Темина. Будучи учеником средней школы в Центральной средней школе в Филадельфии, он участвовал в летней студенческой программе лаборатории Джексона в Бар-Харборе, штат Мэн. Директор программы СиСи Литтл сказал своим родителям, что Темин «несомненно лучший ученый из пятидесяти семи студентов, которые посещали программу с самого начала … Я не могу не чувствовать, что этому мальчику суждено стать. действительно великий человек в области науки ». Темин сказал, что именно его опыт работы в лаборатории Джексона действительно заинтересовал его в науке.
Родители Темина воспитали в своей семье ценности, связанные с социальной справедливостью и независимым мышлением, что проявлялось на протяжении всей его жизни. На бар-мицву Темина семья пожертвовала деньги, которые должны были быть потрачены на вечеринку, в местный лагерь для перемещенных лиц. Темин также был прощальным в своем классе, и он посвятил свою речь актуальным вопросам того времени, включая недавнюю активность водородной бомбы и новости об отправке человека на Луну.
Темин получила степень бакалавра в Свортмор- колледже в 1955 году по специальности биология по программе с отличием. Он получил докторскую степень в области вирусологии животных в Калифорнийском технологическом институте в 1959 году.
Научный вклад
Работа Говарда Темина о вирусах и о том, как они используют клетку-хозяин во время заражения, была чрезвычайно фундаментальной и новаторской в области молекулярной биологии и генетики . Вопреки догме о линейной и однозначной роли поддержки генетической информации, как заявили , от ДНК до мРНК и белков , он подчеркивает в некоторых вирусах роль РНК как носителя генетической информации и ее возможна обратная транскрипция в ДНК с использованием специфического вирусного фермента: обратной транскриптазы . Впоследствии Говард Темин признал приоритет Мирко Белянски в открытии обратной транскриптазы у бактерий. Эти механизмы, специфичные и ограниченные ретровирусом , если они не изменили концепции биологии, но продемонстрировали варианты, особенно позволили необычайному развитию методов молекулярной биологии в годы, последовавшие за использованием в биотехнологии описанных ферментов.
Предпосылки развития гипотезы
РНК — уникальная молекула. Основная ее функция — это связь между геном и белком, она выражена в центральной догме молекулярной биологии: ДНК — РНК — белок. Нужный для синтеза ген, представленный в виде двухцепочечной ДНК, служит матрицей для создания одноцепочечной РНК, точно повторяющей структуру этого гена и способной перенести инструкцию по сборке белка из ядра в цитоплазму клетки. В цитоплазме РНК «находит» рибосому — молекулярную «машину» для синтеза белка. Рибосома, «читая» нуклеотиды в РНК, подбирает для будущего белка аминокислоты согласно генетическому коду — почти каждому триплету (то есть трем нуклеотидам) соответствует какая-то аминокислота (есть еще несколько стоп-кодонов, прерывающих синтез белка, и старт-кодон, с которого всё начинается). Так, нанизывая аминокислоту за аминокислотой, рибосома формирует белок. И если раньше считалось, что РНК — это просто помощник, то за последние годы появилось много данных, опровергающих ее подчиненное положение. Вполне возможно, что РНК не серая мышь рядом со своей куда более известной сестрой, а серый кардинал за ее троном.
Оказалось, что РНК не только играет роль посредника между ДНК и синтезом белка, но и обладает каталитической активностью, то есть может работать как фермент.
Обнаружили каталитическую активность практически случайно. Американцы Томас Чек и Сидни Альтман вообще-то просто изучали таинственные ферменты, в которых анализ показал наличие РНК. Зачем в ферментах РНК? Белок и нуклеиновую кислоту «разделили» и… неожиданно отметили, что и лишенная белка РНК справлялась со своей каталитической функцией. Сначала биохимики подумали, что это ошибка, артефакт, оставшийся или занесенный извне белок — но и искусственно созданная РНК с той же последовательностью работала как фермент. Стало понятно, что ферментативная активность больше не прерогатива белков.
Дальше — больше. Помимо каталитической активности удалось обнаружить еще одно свойство — это регулирование экспрессии генов, то есть степени их проявления. Этот процесс называется РНК-интерференцией, и участвуют в нем, конечно, не все типы РНК, а только два подтипа — микроРНК и малые интерферирующие РНК. Даже сейчас известны тысячи различных РНК, участвующие в подавлении активности гена на всех стадиях его проявления, от считывания ДНК до непосредственного белкового синтеза. Причем оказалось, что интерферирующая РНК может быть даже… двухцепочечной.
Простыми словами интерференцию можно объяснить так: маленькие молекулы РНК комплементарны тем генам, которые нужно заглушить или каким-то другим образом повлиять на их активность, и благодаря таким РНК-«ориентировкам» ферменты-киллеры могут найти уже синтезированную матричную РНК, то есть копию гена, по которой будет работать рибосома, и уничтожить ее. На самом деле механизм, конечно, сложнее, но смысл один — регуляция работы ДНК.
Особенно часто такие РНК проявляют себя в различных процессах, направленных на защиту организма, — они устраняют опасность, уничтожая нуклеиновые кислоты патогенов. Причем этот механизм достаточно древний — он есть у растений и даже, судя по всему, у одноклеточных, по крайней мере микроРНК у некоторых из них уже обнаружили.
Но есть нюанс
Гипотеза РНК имеет обширную доказательную базу и по праву считается одной из самых логичных и подходящих для объяснения формирования жизни. Но и у нее есть недостатки, или, вернее, вопросы, ответы на которые в рамках самой гипотезы найти сложно.
Во-первых, РНК очень нестабильна, а время ее жизни крайне ограничено. Сложно представить себе «начало начал», способное распасться при малейших изменениях в окружающей среде. РНК нуждается в ионах двухвалентных металлов, в основном в магнии, но при этом распадается при их слишком большой концентрации. РНК любит кислую среду, но практически не выдерживает щелочной.
Во-вторых, много вопросов и к самому «случайному» синтезу. Да, сахара действительно могли быть занесены извне, и да, протонуклеотиды действительно могли быть синтезированы из «того, что было». Но вот представить себе синтез итоговой молекулы РНК сложно — слишком много условий должно было совпасть для этого (та же рибоза если и была занесена из космоса, то явно в очень малых количествах). Экспериментально, впрочем, возможность соединения сахара и нуклеотида уже была показана, но ведь есть и третий участник — остаток фосфорной кислоты, и о его ранней судьбе данных пока нет. Всё это привело к тому, что из гипотезы РНК-мира возникла подгипотеза — пре-РНК-мира: в начале появились первичные метаболические компартменты-протоклетки, а потом уже в них пошел синтез реплицирующихся молекул РНК, где возникали все возможные варианты соединения трех участников, пока не был найден единственный верный.
В-третьих, возникает вопрос о формировании протоклетки. Да, мембрана очень полезна — она защищает хрупкую РНК, позволяя ей «жить» чуть дольше, чем просто в обычном растворе. Но точно так же она отделяет РНК от необходимых ей элементов — нуклеотидов и ионов. То есть для формирования первых бислоев с включенной в них РНК уже должны были появиться какие-то простые системы закачки или хотя бы связывания нужных элементов, своего рода первичные челночные системы. Даже это в целом представить можно, но каким образом РНК координировала их работу?
Из предыдущего вопроса вполне логично вытекает следующий: каким образом эти белки оказались встроены в мембрану, а главное — как появился генетический код, позволяющий синтезировать эти белки?
Евреи в науке: вклад и достижения
Евреи сыграли центральную роль в многих научных открытиях и достижениях XX и XXI веков. Это особенно заметно в областях физики, химии и медицины, где еврейские ученые получили множество Нобелевских премий.
Физика
Еврейские физики, включая таких выдающихся ученых, как Альберт Эйнштейн и Ричард Фейнман, сделали важные открытия, которые положили основу для современной физики. Их вклад включает разработку теории относительности, квантовую механику и многие другие ключевые области.
Химия
В области химии евреи также внесли значительный вклад. Примерами служат Аарон Чичановер и Авраам Хершко, израильские ученые, которые получили Нобелевскую премию по химии в 2004 году за открытие убиквитин-протеасомного пути, который играет ключевую роль в регулировании белков в наших клетках.
Медицина или физиология
В области медицины и физиологии евреи также имеют ряд выдающихся достижений. Это включает работу Селига Перуца, который выиграл Нобелевскую премию по химии в 1962 году за работу над структурой гемоглобина, и Эмильу Адаму, который получил Нобелевскую премию по медицине в 2013 году за открытие механизмов регулирования внутриклеточного транспорта.
Литература
В области литературы евреи также достигли выдающихся успехов. Боб Дилан, Американский поэт, певец и композитор еврейского происхождения, стал лауреатом Нобелевской премии по литературе в 2016 году, что доказало его неоспоримое влияние на музыку и культуру. Прозаик и поэт, Сауль Беллоу, получивший премию в 1976 году, также был евреем.
В начале была РНК
Университет Иллинойса, 1967 год. Молодой, ему всего 39 лет, профессор Карл Вёзе занимается делом всей своей жизни — молекулярной эволюцией. В какой-то момент Вёзе заметил, что маленькие РНК, участвующие в создании рибосом («машин» по сборке белка на основе генетического кода), — очень удобный материал для изучения мутаций и изменений, возникающих от вида к виду. Это своеобразные хронометры, и Вёзе решил прибегнуть к ним для изучения филогенетических, то есть эволюционных, деревьев.
Вообще-то Вёзе хотел опровергнуть довлеющую теорию о том, что археи суть изменившиеся бактерии. Он считал, что всё живое можно разделить на три независимых домена — археи, бактерии и животные — и что археи не просто «странные бактерии», а целое отдельное царство, развивающееся по собственному пути. В конце концов, ему это удалось, но параллельно с открытием доменной структуры жизни Вёзе, всю жизнь изучавший РНК, пришел к неожиданному выводу.
Вёзе писал:
И вот накопленные знания об РНК, ее свойствах и способности изменяться наталкивают Вёзе на мысль, что именно РНК была тем «посредником» между миром неорганических молекул и жизнью. В этом ему сильно помогает открытие у РНК способности к катализу — то, что раньше считалось только белковой привилегией, оказывается вовсе не редкостью для маленьких нуклеиновых кислот.
Обрастать плотью доказательств гипотеза стала позже, с приходом на мировую научную арену новых молекулярных биологов, в частности Уолтера Гилберта. Он занимался разработкой методов секвенирования — расшифровки нуклеотидной последовательности и за это в 1980 году получил Нобелевскую премию вместе с Полом Бергом. Но, как любой крупный ученый, Гилберт интересовался многим и в 1986 году опубликовал статью, развивающую идеи Вёзе, — «Происхождение жизни. РНК-мир». Именно Гилберт придумал для гипотезы емкое название — РНК-мир.
Все полученные данные об РНК неплохо укладывались в эту теорию. Даже организмы, содержащие только РНК без присутствия ДНК, нашлись — РНК-вирусы, обширная группа, включающая и представителей семейства коронавирусов. Нашлись и косвенные подтверждения гипотезы в самой молекулярной догме и процессах репликации (то есть удвоения) ДНК
Дело в том, что если рассматривать всех участников молекулярной догмы, то можно заметить одну важную деталь: рибосомы для синтеза белка есть у всех и в целом очень похожи по строению — не важно, у кого мы будем брать рибосому, у архей, бактерий или эукариот. Та же ситуация с процессом снятия копии, то есть синтеза матричной РНК
А вот участники процесса репликации ДНК немного разнятся у разных царств, хотя процесс идейно похож. Из этого наблюдения у ряда ученых родилось любопытное предположение: репликация ДНК появилась позже рибосом и системы синтеза РНК, хотя четких доказательств пока нет.
Краткий Обзор
Нобелевская премия была учреждена в 1895 году в завещании шведского изобретателя и промышленника Альфреда Нобеля
С тех пор она стала важнейшим событием в глобальной научной, литературной и мировой общественной сферах, предоставляя признание и внимание важным достижениям и вкладу в общество. Целью этой статьи является исследование того, как евреи вписываются в эту историю, и их вклад в различные области, которые Нобелевская премия признает
Альберт Абрахам Михельсон, уроженец Польши и эмигрант в США, стал первым евреем, удостоенным Нобелевской премии. Его приз за физику в 1907 году был результатом его точных измерений скорости света. Михельсон был только началом удивительной истории вклада евреев в области, признанные Нобелевской премией.
На протяжении XX века множество евреев получило признание своих достижений в виде Нобелевской премии. От научных открытий в физике и медицине до литературных произведений и усилий по миру, эти лауреаты значительно повлияли на мир.
Исключения из догмы
Так называемые «исключения из догмы» скорее являются ее дополнением. Если в рамках догмы рассмотреть, что происходит с биологическими объектами, которые мы называем вирусами, картина немного меняется.
Верно, что в клеточных организмах вся генетическая информация кодируется в виде двухполосных молекул ДНК, которые дублируются путем репликации (ДНК → ДНК). Но в мире вирусов мы находим геномы, состоящие не только из ДНК, но и из РНК.
Некоторые из этих РНК производят собственные копии в процессе репликации РНК (т.е. РНК → РНК). Ферменты, отвечающие за этот процесс, называются репликазами РНК.
С другой стороны, хотя верно, что части ДНК могут быть транскрибированы в молекулы РНК посредством транскрипции (ДНК → РНК), возможно и обратное.
То есть есть молекулы РНК, которые можно (ретро) транскрибировать в ДНК посредством процесса обратной транскрипции (РНК → ДНК). Эта ферментативная активность осуществляется обратной транскриптазой.
Наконец, как мы уже упоминали, не все гены кодируют пептиды, и не все РНК являются мРНК.
Верно то, что они являются наиболее «важными», поскольку порождают исполнителей функций в ячейке. То, что пептиды (а также гомо- и гетеропептидные белки) очень сложны в информационном отношении, также верно. Но без других РНК, не являющихся мРНК, жизнь была бы невозможна.
Кроме того, существуют транскрипты РНК, которые сами по себе обладают ферментативной активностью (рибозимы или РНК с каталитической активностью). В этом случае получение пептида не является конечной информационной целью.
– Транскрипты РНК, несущие послание пептида и других биомолекул
Второй постулат догмы гласит, что ген, кодирующий пептид, транскрибируется РНК-полимеразой (транскриптазой) в информационную РНК (мРНК), то есть ДНК → РНК. Но ДНК также кодирует другие функциональные биомолекулы, не являющиеся пептидами.
Эти гены также подвергаются транскрипции с помощью специфических РНК-полимераз, в результате чего возникают РНК, выполняющие свою собственную функцию.
Например, рибосомы состоят как из белков, так и из молекул РНК. Молекулы рибосомной РНК кодируются в ДНК в так называемых рибосомных генах (рДНК).
Существует огромное количество РНК, которые выполняют свои функции сами по себе, не нуждаясь в трансляции. Все они закодированы в ДНК.
Эти РНК включают, среди прочего, РНК-переносчики, каждая из которых кодируется собственным геном, малые ядерные РНК, малые ядрышковые РНК, микроРНК и т. Д.
Типы передачи информации
Виды передачи последовательной информации, разрешенные согласно Центральной догме. Доказательств передачи, представленных пунктирными стрелками в 1958 г., не было.
Согласно Крику (1970), девять теоретически возможных типов передачи последовательной информации между ДНК, РНК и белком можно разделить на три области: общие типы передачи происходят в каждой клетке за редкими исключениями. Известно о существовании особых типов передачи, но они происходят только при определенных условиях / у определенных организмов. С другой стороны, существование остальных типов передачи не могло быть показано до сегодняшнего дня и опровергло бы центральную догму.
Общие виды трансмиссии
- ДНК → ДНК: репликация
- ДНК → РНК: транскрипция
- РНК → белок: перевод
Специальные виды трансмиссии
- РНК → РНК: репликация РНК , например, происходит. B. в РНК-вирусах (пример: полиовирус ) РНК-зависимыми РНК-полимеразами и вироидах
- РНК → ДНК: обратная транскрипция , например Б. в ретровирусах с помощью фермента обратной транскриптазы или в эукариотах с помощью теломеразы
- ДНК → белок: прямая трансляция ДНК в белок была продемонстрирована in vitro в бесклеточной среде.
Неизвестные способы передачи запрещены Центральной Догмой
- Белок → ДНК
- Белок → РНК
- Белок → белок
Жизнь и карьера после Нобелевской премии
После получения Нобелевской премии в 1975 году Темин прошел путь от бунтаря в научном сообществе до весьма уважаемого исследователя. Темин начал получать международное признание за свою работу и использовал свою недавно приобретенную известность для улучшения мира. Примером этого был октябрь 1976 г .; Темин помогала ученым в Советском Союзе, которые были мишенью КГБ, секретной полиции в Советском Союзе. Советские ученые-евреи были лишены работы и подвергнуты притеснениям после того, как запросили визы для эмиграции в Израиль. Темин поставил перед собой задачу лично посетить ученых и их семьи. Он дарил им подарки, которые можно было перепродать, чтобы помочь им материально, и он раздал ученым копии научных журналов, которые были запрещены КГБ. Однажды Говард Темин прочитал лекцию некоторым советским еврейским ученым в чьем-то доме. На следующее утро почти все ученые, присутствовавшие на лекции, были арестованы. После того, как они были освобождены, Темин записал на пленку один из рассказов ученого об этом событии и передал пленку газетам в Соединенных Штатах, чтобы информация о ситуации, в которой оказались еврейские ученые, была опубликована.
Еще один пример попытки Темина улучшить мир — это прием Нобелевской премии . После получения Нобелевской премии от короля Швеции Карла Густава; Темин обратился к курильщикам в аудитории, в том числе к королеве Дании , и сказал, что он «возмущен тем, что одна из основных мер, доступных для предотвращения многих видов рака, а именно отказ от курения, не получила широкого распространения». Он также настоял на том, чтобы убрать пепельницу, находящуюся на столе лауреатов.
После получения Нобелевской премии Темин также стал более активным в научном сообществе, помимо исследований. Он был участником более 14 научных журналов. В 1979 году он стал членом-консультантом директора Национального института здоровья (NIH) и членом подгруппы генной терапии человека консультативного комитета по рекомбинантной ДНК. Он также был членом Национального консультативного совета по раку и председателем подкомитета по СПИДу. В Национальном институте аллергии и инфекционных заболеваний (NIAID) он был председателем консультативного совета по генетическим вариациям по развитию СПИДа и был членом консультативного совета по вакцинам. В Национальной академии наук (NAS) он был членом комитета премии Ваксмана и комитета по обзору отчетов. В 1986 году Темин стал членом комитета Института медицины (IOM) / NAS по национальной стратегии по вопросам государственной политики, связанным со СПИДом. Последним комитетом, в котором работал Темин, был Консультативный совет Всемирной организации здравоохранения .
В 1981 году Темин стал одним из основателей Всемирного культурного совета .
Внешние ссылки
- Авторитетные записи :
- Ресурс исследования
(en + ja + zh-Hans + zh-Hant + ru) Scopus
:
|
Лауреаты Нобелевской премии по физиологии и медицине |
|
|---|---|
| 1901-1925 гг. |
|
| 1926-1950 гг. |
|
| 1951-1975 |
|
| 1976-2000 гг. |
|
| 2001-настоящее время |
|
|
Редактирование генов в России
Целью эксперимента российского биолога будет модификация того же гена, над которым работал китайский специалист по генной инженерии – CCR5. В интервью Nature Ребриков рассказал, что собирается отключить ген в эмбрионах, который кодирует белок, позволяющий ВИЧ проникать в клетки организма. Эмбрионы впоследствии будут имплантированы ВИЧ-позитивным матерям, которые не реагируют на стандартную терапию. Отмечается, что риск передачи инфекции ребенку в этом случае будет выше, но если в ходе процедуры получится успешно отключить ген CCR5, то этот риск будет значительно снижен.
Напомним, что Хэ Цзянькуй в свою очередь брал клетки ВИЧ-положительных отцов, а затем пересаживал полученные эмбрионы ВИЧ-отрицательным матерям. В этом не было никакого практического смысла, что в свою очередь помимо прочего являлось еще одной причиной критики китайского генетика мировым сообществом ученых. Работа Хэ вызывала шквал критики среди научного сообщества и привела к появлению открытого письма, в котором ученые призвали к мораторию на проведение экспериментов по генному редактированию эмбриональных клеток. Ребриков утверждает, что его метод модификации гена окажется полезнее, будет менее рискованным и более этически оправданным и приемлемым для общества.
Ребриков добавляет, что уже достиг соглашения с местным ВИЧ-центром, где он собирается привлечь женщин добровольцев, готовых принять участие в его эксперименте.
Журнал Nature обратился за комментариями по поводу планируемого эксперимента российского ученого к другим исследователям, которые, как и ожидалось, выразили обеспокоенность планами Ребрикова. Например, Дженнифер Дудна, специалист по молекулярной биологии из Калифорнийского университета в Беркли и один из пионеров метода генного редактирования CRISPR-Cas9 говорит, что данная технология еще до конца не изучена и не готова для применения в клинических ситуациях.
Даже если опыт пройдет успешно, небольшой риск заражения останется. И до сих пор мы точно не знаем, как это отразится на жизни человека в целом. Например, в недавнем исследовании у носителей обеих копий мутантного CCR5 нашли риск более ранней смерти по сравнению с носителями нормального гена.
Российские специалисты также выразили свое несогласие с подобными экспериментами.
Молекулярный генетик Константин Северинов, с которым связались авторы Nature отметил, в России получить одобрение на проведение подобных экспериментов будет очень сложно. Ведь придется учитывать не только мнение государственных структур, но и церкви, которая выступает против редактирования генов. А это сильно сокращает шансы получить одобрение – по крайней мере в ближайшие годы.
И все же самый важный вопрос — насколько реальна перспектива, которую рисует Ребриков?
Долотовский считает, что эксперимент технически провести возможно, но проблема заключается в этической части вопроса.
По словам самого Ребрикова, к которому редакция Hi-News.ru обратилась за комментариями, этическая сторона вопроса – крайней важный аспект.
Что такое РНК
РНК (рибонуклеиновая кислота) — это такая же нуклеиновая кислота, как и ДНК, и во многом она очень похожа на свою более известную родственницу. В отличие от ДНК РНК обычно не формирует двойные спирали, хотя и они, и другие сложные структуры у нее иногда встречаются. Состоит РНК из почти тех же самых «единиц», или азотистых оснований: если в ДНК встречаются аденин, гуанин, тимин и цитозин, то в РНК тимин заменяется на урацил. Кроме этого отличаются сахара: в РНК это рибоза (отсюда и буква Р в аббревиатуре), а в ДНК дезоксирибоза. Азотистое основание и сахар (их совокупность называется сахаро-фосфатным остовом) составляют своего рода кирпичик для построения нуклеиновой кислоты, и они, соединяясь друг с другом через остаток фосфорной кислоты, формируют итоговую полимерную цепь.
История изучения РНК походит то на мелодраму, то на детектив. Впервые она была выделена в далеком 1868 году. Тогда швейцарский физиолог Иоганн Фридрих Мишер выделил ее вместе с ДНК в виде непонятного нового вещества, которое он назвал нуклеином — в честь клеточного ядра (по-латински nucleus). Первоначально ученые вообще не считали ДНК и РНК хоть как-то связанными друг с другом — вплоть до того, что ДНК называли нуклеином тимуса, а РНК нуклеином дрожжей. Потом удалось выяснить состав сахаров, и РНК получила свое современное название.
Карьера
В 1960 году Хауард Мартин Темин был назначен доцентом лаборатории Макардла по исследованию рака в Университете Висконсин-Мэдисон. Именно здесь он начал работать над новаторскими исследованиями, которые привели к формулировке гипотезы ДНК-провируса.
В последующие годы он поднялся по служебной лестнице, последовательно становясь адъюнкт-профессором, ординарным профессором и профессором исследований рака Фонда выпускников Висконсина. В 1974 году он стал профессором вирусной онкологии и клеточной биологии Американского онкологического общества.
В 1960-х он сосредоточился на изучении вируса саркомы Рауса. Его исследования по контролю размножения неинфицированных и инфицированных вирусом саркомы Рауса клеток в культуре привели его к открытию обратной транскриптазы (RT) — фермента, используемого для генерации комплементарной ДНК (кДНК) из матрицы РНК.
Первоначально его открытие подверглось критике со стороны выдающихся ученых, поскольку идея RT противоречила центральной догме молекулярной биологии, согласно которой ДНК транскрибируется в РНК, которая затем транслируется в белки. Примерно в то же время другой ученый, Дэвид Балтимор, независимо выделил ОТ из двух РНК-опухолевых вирусов, и концепция ОТ начала получать признание.
За свои открытия Темин получил долю лауреата Нобелевской премии 1975 года по физиологии и медицине. Его высокий статус всемирно уважаемого ученого побудил его стать более активным в научном сообществе, помимо исследований.
В 1979 году Хауард Мартин Темин стал членом-консультантом директора Национального института здоровья (NIH). В том же году он также стал членом подгруппы генной терапии человека Консультативного комитета по рекомбинантной ДНК. Он был научным сотрудником Американской академии искусств и наук, а также членом Национальной академии наук.
Ранняя жизнь
Хауард Мартин Темин родился в Филадельфии 10 декабря 1934 года в семье евреев. Его мать, Аннетт Леман, была активисткой, которая часто занималась вопросами образования, а его отец, Генри Темин, был адвокатом. У Хауарда было два брата.
Во время учебы в Центральной средней школе в Пенсильвании он участвовал в летней студенческой программе лаборатории Джексона в Бар-Харборе, где проявил необычайные способности к науке. Он также провел лето в Институте исследования рака в Филадельфии.
Он поступил в Swarthmore College в 1951 году и окончил его в 1955 году со степенью бакалавра по специальности биология по программе с отличием. Затем он приступил к изучению экспериментальной эмбриологии в Калифорнийском технологическом институте в Пасадене. Через несколько месяцев он сменил специальность на вирусологию животных, став аспирантом лаборатории профессора Ренато Дульбекко.
В институте на него большое влияние оказали профессор Макс Дельбрюк и доктор Мэтью Мезельсон. Темин получил докторскую степень. получил степень в области вирусологии животных в 1959 году и проработал дополнительный год в лаборатории профессора Дульбекко в качестве постдокторанта.
Знаменитые Евреи — лауреаты Нобелевской премии
Альберт Эйнштейн
Возможно, самым известным еврейским лауреатом Нобелевской премии является Альберт Эйнштейн, который получил Нобелевскую премию по физике в 1921 году за объяснение фотоэлектрического эффекта.
Нильс Бог
Нильс Бог, отец квантовой механики, был евреем по матери. Он получил Нобелевскую премию по физике в 1922 году за исследования в области структуры атомов и излучения, что оказало глубокое влияние на развитие физики.
Боб Дилан
Как уже упоминалось, Боб Дилан получил Нобелевскую премию по литературе в 2016 году, став первым музыкантом, который получил эту премию за создание нового поэтического выражения в рамках большой американской песенной традиции.
Эли Визель
Эли Визель был автором, активистом прав человека и профессором. Он был награжден Нобелевской премией мира за свои усилия в борьбе за мир, гуманизм и права человека.
























